本文约8778字,阅读大约需要21分钟

前 言
近日,最高人民法院(“最高院”)针对替格瑞洛晶型专利无效的行政诉讼做出二审判决((2019)最高法知行终33号),该二审判决改变了无效决定和一审判决关于不予接受补充实验数据的认定(即,二审判决接受了阿斯利康公司提交的补充实验数据)。不过,二审判决并未认为一旦接受补充数据,即可证明创造性。而是基于补充实验数据与涉案专利的记载不一致,以及在没有进一步证据的情况下,难以证明所述技术效果达到了本领域技术人员预料不到的程度,仍然认定涉案专利不具有创造性,基于此,驳回阿斯利康公司的上诉,维持无效决定和一审判决。至此,国家知识产权局于2017年11月22日做出的宣告ZL200610002509.5全部无效的第33975号决定现已生效。
该二审判决应当是适用《最高人民法院关于审理专利授权确权行政案件适用法律若干问题的规定(一)》(“专利确权司法解释(一)”)第十条“补充实验数据”的首份判决,且基于“原专利申请文件应当明确记载或者隐含公开了补充实验数据拟直接证明的待证事实”和“申请人不能通过补充实验数据弥补原专利申请文件的固有内在缺陷”这两方面,对补充实验数据是否应当被接受进行了全面详尽分析。该二审判决将直接影响后续涉及补充实验数据的认定,并进而影响创造性的认定,相信该二审判决的作出,将引发同行的深入学习和解读。
壹、二审判决简析
1.关于阿斯利康公司提交的补充实验数据是否应当被接受
专利确权司法解释(一)第十条规定,对于专利申请人在申请日之后提交的补充实验数据,应当予以审查。
首先,原专利申请文件应当明确记载或者隐含公开了补充实验数据拟直接证明的待证事实,此为积极条件。既不能仅仅因为原专利申请文件记载了待证事实而没有记载相关实验数据,即推定申请人构成以获取不当利益为目的的不实记载,当然拒绝接受有关补充实验数据;也不能以申请人或有可能作不实记载为由,当然地要求其所提交的补充实验数据形成于申请日或者优先权日之前。
其次,申请人不能通过补充实验数据弥补原专利申请文件的固有内在缺陷,此为消极条件。意在强调补充实验数据通常应当通过证明原专利申请文件明确记载或者隐含公开的待证事实具备真实性,进而对申请人或者专利权人最终要证明的法律要件事实起到补充证明作用,而非独立证明原专利申请文件中未予公开的内容,进而克服原专利申请文件自身公开不充分等内在缺陷。
2.关于阿斯利康公司提交的补充实验数据是否能够证明权利要求1所述晶型的化合物具有预料不到的技术效果
以权利要求1化合物和证据6实施例32相比,尽管权利要求1化合物在两项稳定性指标上都优于证据6实施例32,但尚不能由此认定,权利要求1化合物在代谢稳定性方面的更优效果达到了本领域技术人员预料不到的程度。
根据二审查明的事实,证据6实施例32已经具备药物稳定性;而反证2中文译文第6页记载了一项“令人惊讶的”技术效果,但第7页记载的涉及本专利权利要求1化合物的代谢稳定性仅为“可接受的”。显然,反证2记载的涉及本专利权利要求1化合物的代谢稳定性与本专利说明书的记载在程度上不尽一致。综合考虑上述证据,尽管权利要求1化合物的代谢稳定性优于证据6实施例32,但在没有进一步证据的情况下,难以证明该技术效果达到了本领域技术人员预料不到的程度。
3.关于本专利权利要求1实际解决的技术问题
鉴于补充提交的实验数据,亦不能证明本专利权利要求1的化合物具有“令人惊讶的高代谢稳定性和生物利用率”,故所谓提高具有作为P2T受体(P2YADP或P2TAC)拮抗剂的效能、代谢稳定性和生物利用率这一技术问题并不存在,本专利权利要求1实际解决的技术问题仍仅为提供一种具有便于操作和加工的结晶化合物,被诉决定和原审判决对这一问题认定的结论正确。
4.关于化合物结构和晶型的创造性问题
与无效决定和一审判决的认定相同,本专利化合物的结构和晶型均不具有创造性。此外,被诉决定和原审判决先讨论化合物的创造性,再讨论该化合物某一晶型的创造性,符合研发实践,且符合创造性的整体判断原则。
贰、药品简介
替格瑞洛(Ticagrelor)是由阿斯利康公司研制开发的一种新的治疗急性冠脉综合征的抗血小板聚集药,于2010年12月在欧洲上市,于2011年7月被美国FDA批准上市,上市后被众多国际治疗指南推荐用于ACS患者的治疗,包括欧洲心脏病学会ESC指南、美国心脏病学会ACC指南和美心脏协会AHA指南等,2012年11月替格瑞洛获准在中国正式上市。目前已在包括美国在内的85个国家批准上市。据报道,替格瑞洛相对氯吡格雷具有如下优势:一是直接对P2Y12受体快速产生抑制效应而不需经代谢活化,相比氯吡格雷能更强效抑制血小板聚集;二是可逆性,抑制程度反映血浆浓度,在停药后循环中所有血小板均可恢复功能。
叁、第33975号无效决定简析
无效决定涉及ZL200610002509.5权利要求1保护:一种结晶态形式为晶型II的式(I)化合物(下称“替格瑞洛晶型”):
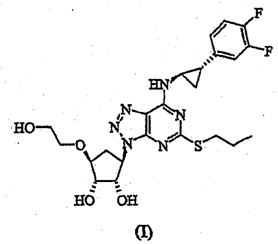
其特征在于,X-射线粉末衍射图基本上如图1.2所示。
1.关于显而易见性
将权利要求1保护的替格瑞洛晶型与证据6实施例32的下述结构相比,其区别在于:
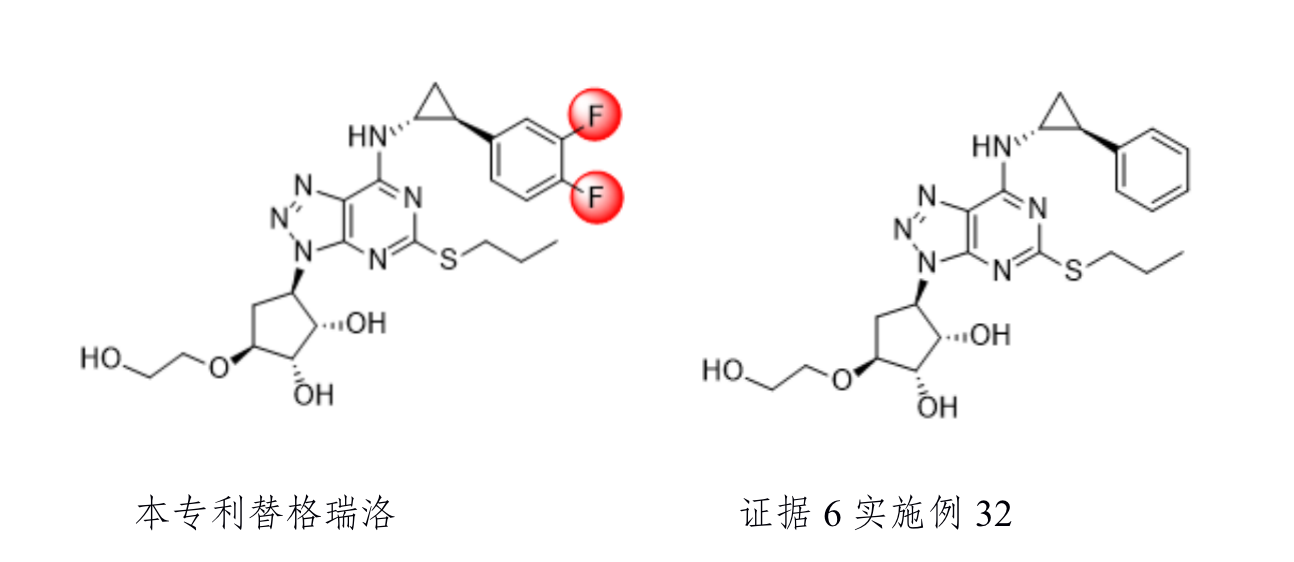
(1)化合物本身结构存在差异,权利要求1化合物的右侧苯环上具有3,4-二氟取代基,证据6化合物的右侧苯环上无取代基;
(2)权利要求1化合物为具有特定X-射线粉末衍射图的晶型II,证据6没有提及化合物的状态。
● 关于发明实际要解决的技术问题
本专利声称其相对于证据6实际解决的技术问题为,提高具有作为(P2YADP或P2TAc)拮抗剂的效能、代谢稳定性和生物可利用率,并且使得化合物在药物制备中更方便操作和加工。
证据3(WO0034283A1,并非本专利的现有技术,该专利无效案目前在再审程序中)实施例3制备了替格瑞洛化合物,但证据3也没有记载本专利化合物在代谢稳定性和生物利用率方面具有何种技术效果,本领域技术人员从证据3获得的教导是其pIC50应当大于5.0,即与证据6化合物处于相同的拮抗水平上。
反证5提供了如下对比实验数据:
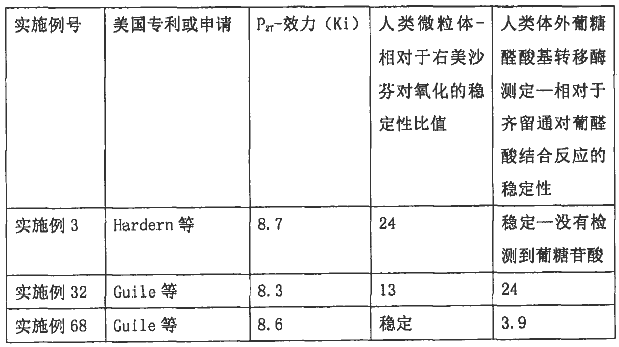
从P2T效力(Ki)的试验结果来看,证据3实施例3优于证据6实施例32,但与证据6实施例68处于基本相同的水平;人类微粒体-相对于右美沙芬对氧化的稳定性试验中,证据3实施例3优于证据6实施例32,但逊于证据6实施例68;而人类体外葡糖醛酸基转移酶测定-相对于齐留通对葡醛酸结合反应的稳定性试验中,证据3实施例3优于证据6实施例32以及证据6实施例68,专利权人在口头审理过程中对上述事实也予以确认。可见,由于上述三个实施例化合物在不同的试验中表现各异,没有证据表明本领域技术人员能够根据上述试验结果直接地、毫无疑义地确定哪个化合物的表现最佳,因此,上述试验结果不能用于证明本专利化合物相对于证据6化合物在代谢稳定性和生物利用率方面具有更好的技术效果。
关于结晶化合物较之无定型化合物稳定性好,便于操作和加工的优点,本领域技术人员公知这是结晶化合物所具备的常规优势,本专利说明书也没有提供任何试验数据,以表明本专利保护的晶型II较之常规结晶化合物具备何种预料不到的技术效果。
因此,本专利权利要求1相对于证据6实际解决的技术问题仅为提供一种具有便于操作和加工的结晶化合物。
对于区别(1)
即化合物本身结构的差异,证据6实施例68给出了类似化合物的右侧苯环上具有3,4-二氟取代基的明确教导,在实施例32和68化合物的主体结构如此接近,并具有相同技术效果的情况下,本领域技术人员有动机进行这种苯基上卤素原子的取代以获得结构类似的化合物,并预期取代后的化合物仍然具有类似的拮抗功能。
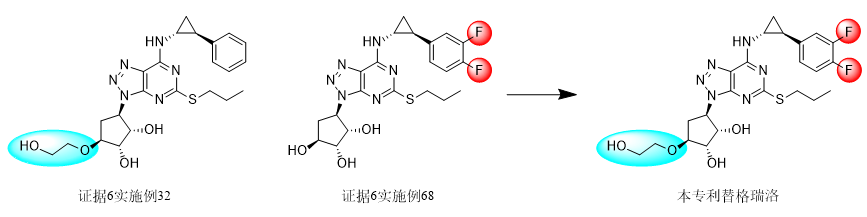
对于区别(2)
在制药领域,药物的稳定性和加工性能是药物活性物质被发明后在其最终成为药品的过程中所要解决的技术问题。众所周知,晶体是内部的构造质点(如原子、分子)呈平移周期性规律排列的固体,并具备晶格能,与具有相同化学成分的非晶体相比,晶体更具稳定性,流动性更好因而更加便于加工,因此,本领域技术人员在面对现有化合物不能令人满意的性能时,有动机对该化合物进行结晶化的实践尝试,继而对所获晶体的具体技术参数(例如X射线颜色图谱)进行测定。
综上,本领域技术人员有动机并且有能力利用常规的晶体制备的实验手段来完成将化合物转化为晶型的实践尝试,继而对所获晶体的具体技术参数(例如X射线衍射图谱)进行测定,从而形成本专利权利要求1的技术方案。因此权利要求1相对于证据6和证据4的结合不具备创造性。
肆、一审判决简析
北京知识产权法院于2019年2月25日针对上述无效决定作出一审判决(案号:(2018)京73行初2034号行政判决),其认为,(1)对于结构差异和晶型的区别,坚持无效决定的认定;(2)对于该区别特征所能达到的技术效果。首先,阿斯利康公司称反证5的实验数据能够证明权利要求1实际解决的技术问题是使化合物的代谢稳定性更高,但是,反证5的实验数据是在本专利的申请日后完成的,本专利仅在说明书的“背景技术”部分声称“所述化合物作为P2T受体(P2YADP或P2TAc)拮抗剂呈现出高的效能。并且还具有令人惊讶的高代谢稳定性和生物可利用率”,说明书其他部分均未再提及本专利所述化合物的代谢稳定性,亦未给出任何有关代谢稳定性的实验数据,即阿斯利康公司声称的代谢稳定性等方面的技术效果在本专利说明书中并未明确记载,本领域技术人员也无法根据现有技术确认本专利具有高代谢稳定性等的技术效果。另外,反证5系证人自行完成的实验,而其与阿斯利康公司存在利害关系,且实验条件和实验数据的具体情况并无其他证据佐证。因此,本案不能基于反证5所记载的技术效果来确定本专利实际解决的技术问题,而应当综合本专利说明书所记载的整体内容、现有技术以及本领域技术人员的通常认知来确定本专利权利要求1实际解决的技术问题。
综上所述,原审判决认定无效决定关于权利要求1-4相对于证据6与证据4的结合不具备创造性的认定,结论正确,依法应予支持。
伍、二审判决简析
(一)关于权利要求1实际解决的技术问题
被诉决定认为:本专利相对于证据6实施例32实际解决的技术问题仅为提供一种具有便于操作和加工的结晶化合物。原审判决认为:本专利权利要求1实际解决的技术问题是提供一个与证据6实施例32化合物结构相似的活性化合物并将之制备成特定的晶型以便于后续的操作和加工。阿斯利康公司上诉主张:本专利说明书明确记载了权利要求1的化合物具有“令人惊讶的高代谢稳定性和生物利用率”,阿斯利康公司提交的补充实验数据(反证2和反证5)应当被考虑,且该补充实验数据可以证明权利要求1的化合物具有所述技术效果。
最高院认为,阿斯利康公司提交的补充实验数据是否能够证明权利要求1化合物具有“令人惊讶的高代谢稳定性和生物利用率”,是确定权利要求1实际解决的技术问题的先决问题。由此涉及有关补充实验数据是否应当被接受和是否能够证明待证事实两个问题。
1.关于阿斯利康公司提交的补充实验数据是否应当被接受
本专利说明书“背景技术”部分0005段记载“所述化合物作为P2T受体(P2YADP或P2TAC)拮抗剂呈现出高的效能。并且还具有令人惊讶的高代谢稳定性和生物可利用率”,但说明书的其他部分未提及上述技术效果,也未提供实验数据证明确实存在上述技术效果。原审判决认定,因上述技术效果仅记载在说明书“背景技术”部分,说明书其他部分未再提及且未提供实验数据,本领域技术人员亦无法根据现有技术确认本专利具有上述技术效果,且阿斯利康公司所提供的补充实验数据反证5形成于申请日之后,反证5系与阿斯利康公司有利害关系的证人自行完成的实验,且缺乏其他证据佐证,不能基于反证5所载技术效果确定本专利实际解决的技术问题。阿斯利康公司上诉主张,本专利说明书明确记载了权利要求1的化合物具有“令人惊讶的高代谢稳定性和生物利用率”,有关补充实验数据应当被接受。
专利确权司法解释(一)第十条规定,药品专利申请人在申请日以后提交补充实验数据,主张依赖该数据证明专利申请符合专利法第二十二条第三款、第二十六条第三款等规定的,人民法院应予审查。最高院认为,基于对现有技术的认知差异、对技术方案发明点的理解不同、对本领域技术人员认知水平的把握不一致等,申请人在原申请文件中未记载特定实验数据的情形恐难避免。例如,就创造性而言,化合物药品的创造性既可以基于化合物本身的结构或者形态,也可以基于化合物药品的药效。其中,药效既可以是药物用途,即适应症;也可以是药物效果,即药物活性、药物毒性、药物稳定性、控释速度等。上述任何一个方面非显而易见的技术贡献,都可以作为确定技术方案实际解决的技术问题的依据,使技术方案满足专利授权的创造性要求,申请人在申请日或者优先权日准确预知发明点存在困难。即便申请人对发明点作出了准确预判,因针对同一技术问题,基于对现有技术的不同理解和对最接近现有技术的不同选择,证明非显而易见技术贡献所需的事实和数据也可能不同。再如,就充分公开而言,由于审查员或者无效宣告请求人对于专利申请文件的理解以及对本领域技术人员认知水平的把握,均可能与专利申请人不同,故其可能因此质疑专利申请是否满足充分公开的要求。上述情况下,专利申请人均需要依靠在申请日或者优先权日之后提交的补充实验数据证明其专利申请符合授权条件。因此,对于专利申请人在申请日之后提交的补充实验数据,应当予以审查。
当然,允许专利申请人在申请日或者优先权日之后提交补充实验数据并对该补充实验数据予以审查,并不意味着该补充实验数据当然可以被接受。鉴于专利申请人可能通过在申请日或者优先权日之后提交补充实验数据,将申请日或者优先权日未公开或者未完成的内容纳入专利权保护范围,就此部分内容不正当地取得先申请的利益,从而违反先申请原则,或者借此弥补原专利申请文件公开不充分等固有内在缺陷,从而妨碍说明书应该充分公开等内在要求的贯彻,故对于补充实验数据的接受应当注意避免上述问题。
首先,原专利申请文件应当明确记载或者隐含公开了补充实验数据拟直接证明的待证事实,此为积极条件。如果补充实验数据拟直接证明的待证事实为原专利申请文件明确记载或者隐含公开,即可认定申请人完成了相关研究,有关补充实验数据的接受不违反先申请原则。申言之,既不能仅仅因为原专利申请文件记载了待证事实而没有记载相关实验数据,即推定申请人构成以获取不当利益为目的的不实记载,当然拒绝接受有关补充实验数据;也不能以申请人或有可能作不实记载为由,当然地要求其所提交的补充实验数据形成于申请日或者优先权日之前。本案中,原申请文件说明书“背景技术”部分第0005段明确记载了补充实验数据的待证事实,即“令人惊讶的高代谢稳定性和生物利用率”。原审判决以该记载位于“背景技术”部分,且原专利申请文件未记载支持这一技术效果的实验数据为由,对阿斯利康公司提交的补充实验数据不予接受,缺乏依据。
其次,申请人不能通过补充实验数据弥补原专利申请文件的固有内在缺陷,此为消极条件。所谓不能通过补充实验数据弥补原专利申请文件的固有内在缺陷,意在强调补充实验数据通常应当通过证明原专利申请文件明确记载或者隐含公开的待证事实具备真实性,进而对申请人或者专利权人最终要证明的法律要件事实起到补充证明作用,而非独立证明原专利申请文件中未予公开的内容,进而克服原专利申请文件自身公开不充分等内在缺陷。本案中,原专利申请文件记载了“令人惊讶的高代谢稳定性和生物利用率”这一技术效果。但本领域技术人员仅根据原专利申请文件无法确定权利要求1的化合物是否确有此效果。阿斯利康公司提供的补充实验数据拟通过证明待证事实的真实性,即权利要求1化合物确有“令人惊讶的高代谢稳定性和生物利用率”,来补充证明最终要证明的法律要件事实,即权利要求1具备创造性,故该补充实验数据并非用于克服原专利申请文件的内在缺陷,应予接受。
此外,原审判决认定不应接受本案补充实验数据的理由还包括反证5系与阿斯利康公司有利害关系的证人自行完成的实验,且缺乏其他证据佐证。对此,最高院认为,药物研发领域,尤其是新药研发中,研发主体相对集中。因此,补充实验数据的来源也相对集中。有关补充实验数据的提供者与专利申请人或者专利权人具有雇佣等利害关系,符合研发规律和研发实践,其不应构成对补充实验数据不予采纳的绝对理由。
综上,原审判决关于不应接受阿斯利康公司提交的补充实验数据的认定错误,最高院予以纠正。
2.关于阿斯利康公司提交的补充实验数据是否能够证明权利要求1所述晶型的化合物具有预料不到的技术效果
最高院认为,预料不到的技术效果应当以最接近现有技术为比对对象,被诉决定将权利要求1化合物、证据6实施例32和证据6实施例68三相比较,确有不当。但仅以权利要求1化合物、证据6实施例32观之,尽管权利要求1化合物在“人类微粒体-相对于右美沙芬对氧化的稳定性比值”和“人类体外葡糖醛酸基转移酶测定-相对于齐留通对葡醛酸结合反应的稳定性”两项指标上都优于证据6实施例32,但尚不能由此认定,权利要求1化合物在代谢稳定性方面的更优效果达到了本领域技术人员预料不到的程度。
根据二审查明的事实,首先,证据6实施例32的“人类微粒体-相对于右美沙芬对氧化的稳定性比值”为13,“人类体外葡糖醛酸基转移酶测定-相对于齐留通对葡醛酸结合反应的稳定性”为24,前者大于10即为稳定,后者大于20即为稳定,故此证据6实施例32已经具备药物稳定性;其次,反证2中文译文第6页记载了一项“令人惊讶的”技术效果,但第7页记载的涉及本专利权利要求1化合物的代谢稳定性仅为“可接受的”。显然,反证2记载的涉及本专利权利要求1化合物的代谢稳定性与本专利说明书的记载在程度上不尽一致。综合考虑上述证据,尽管权利要求1化合物的代谢稳定性优于证据6实施例32,但在没有进一步证据的情况下,难以证明该技术效果达到了本领域技术人员预料不到的程度。
3.关于本专利权利要求1实际解决的技术问题
鉴于补充提交的实验数据,亦不能证明本专利权利要求1的化合物具有“令人惊讶的高代谢稳定性和生物利用率”,故所谓提高具有作为P2T受体(P2YADP或P2TAC)拮抗剂的效能、代谢稳定性和生物利用率这一技术问题并不存在,本专利权利要求1实际解决的技术问题仍仅为提供一种具有便于操作和加工的结晶化合物,被诉决定和原审判决对这一问题认定的结论正确。阿斯利康公司关于被诉决定和原审判决对本专利权利要求1实际解决的技术问题认定错误的上诉主张,缺乏依据,不予支持。
(二)关于本专利权利要求1化合物结构的创造性认定
与无效决定和一审判决认定基本相同,权利要求1的化合物结构不具备创造性。
(三)关于本专利权利要求1晶型的创造性认定
与无效决定和一审判决认定基本相同,权利要求1的晶型不具备创造性。
综上,被诉决定和原审判决关于本专利权利要求1化合物的晶型Ⅱ相对于证据6和证据4的结合不具备创造性的认定,并无不当。
(四)关于被诉决定和原审判决是否违反了创造性的整体判断原则的问题
最高院认为,阿斯利康公司的上述主张缺乏依据,不能成立。首先,本领域技术人员有动机在完成新化合物研发后,利用结晶手段对其进行纯化并获得稳定晶型。通过化学方法合成得到的固体化合物含有一定的杂质,并且该固体化合物尚未形成稳定的晶型,利用结晶的手段对合成得到的化合物进行纯化并获得稳定的晶型是药物化学领域通常的做法;选择合适的药物晶型可以提升药物的稳定性、药物制剂制备工艺的可实施性和质量可控性,并且也能获得良好的生物学活性以及临床治疗效果是本领域公知常识。本领域技术人员完成新化合物药物研发后,继续对其作晶型筛选,实属平常。其次,被诉决定和原审判决先讨论化合物的创造性,再讨论该化合物某一晶型的创造性,符合研发实践,且符合创造性的整体判断原则。根据药物研发的一般规律,完成化合物研发是开展晶体研发的前提。本专利权利要求1确系新化合物的新晶体形式,但结构修饰和晶型筛选亦有先后之分,并非同步进行。被诉决定和原审判决均先认定权利要求1所述新化合物不具备创造性;进而述及该新化合物的新晶体形式针对证据6和证据4的结合不具备创造性,其中证据6主要针对新化合物、证据4主要针对新晶体形式。故被诉决定和原审判决不构成对创造性整体判断原则的违反。
综上,二审判决认为涉案专利不具有创造性。
陆、一点思考
通过对二审判决,尤其是补充实验数据的研读,似乎可以得出如下初步结论:
1.补充实验数据能够接受的前提是,不得违反先申请原则,也不得违反公开充分的要求。即,不应当将申请日或者优先权日未公开或者未完成的内容纳入专利权保护范围;或者借此弥补原专利申请文件公开不充分等固有内在缺陷。
2.如果补充实验数据拟直接证明的待证事实为原专利申请文件明确记载或者隐含公开,即可认定申请人完成了相关研究,有关补充实验数据的接受不违反先申请原则。最高院还进一步指出,如果原专利申请文件没有记载相关实验数据,不能当然拒绝接受有关补充实验数据;也不能以有可能作不实记载为由,当然地要求其所提交的补充实验数据形成于申请日或者优先权日之前。如此的话,是否表明,仅有待证事实而没有相关实验数据,以及该证据形成于申请日后,也存在被接受的可能?如此是否违背了先申请原则?
3.补充实验数据通常应当是通过证明原专利申请文件明确记载或者隐含公开的待证事实具备真实性,进而起到补充证明作用,而不能用于克服原专利申请文件自身公开不充分等内在缺陷。
4. 补充实验数据用于证明创造性时,一方面得要求该补充实验数据和涉案专利记载的程度是一致的,当然还得要求该实验数据所达到的技术效果相较于最接近的现有技术,产生了预料不到的技术效果。就本案而言,本专利记载的是“令人惊讶的”技术效果,而反证2记载的本专利化合物的效果仅证明为“可接受的”。显然,这两者在程度上不尽一致。而且,证据6记载的实验数据已经表明相应化合物具备药物稳定性,故补充实验数据还无法证明其技术效果达到了预料不到的程度。
识别二维码查看相关文件

1.替格瑞洛的新晶形
2.最高法知行终33号-替格瑞洛晶形案