目前发现新的药物活性化合物越来越难,制药企业逐渐转变开发模式,采用包括“老药新用”、“联合用药”、精准医疗下的个体化用药等方式,通过“药物重定位”降低他们的研发成本,尤其是通过“联合用药”充分再利用已有或现有产品结构,延长已开发产品的生命周期。
知元团队曾简单统计过1995-2015年间全球化学药专利的技术研究方向,虽然申请总量最大的技术方向是新化合物及其合成技术,其次是药物新用途、联合应用和药物组合物,但从近十年全球专利申请趋势来看,药物新用途、联合应用和药物组合物显现出年申请量高于新化合物及其合成技术申请量的势头。上述专利申请量的趋势特点,与化学药领域新药开发的形势转变相吻合。
以抗病毒药物为例,病毒是细胞内寄生微生物,研制选择性作用于病毒而不影响宿主细胞的药物很困难,而病毒易变异致药物很快失效,又加剧了可用抗病毒药物数量有限的窘境。因此联合应用针对病毒增殖过程不同环节的抗病毒药,快速抑制甚至清除病毒,避免耐药毒株出现,对改变现有抗病毒药研发局面下的治疗效果具有现实意义。以抗HIV药物为例,目前已上市药物类别有CCR5受体抑制剂、融合抑制剂、蛋白酶抑制剂、整合酶抑制剂、核苷类逆转录酶抑制剂、非核苷类逆转录酶抑制剂,而联合用药(鸡尾酒疗法)已成为HIV研发重点,由后三种抑制剂组成的疗法又是联合用药中的主流选择。
吉利德科学公司(Gilead Sciences, Inc.)是一家致力于研究、开发抗病毒药物的公司,其在近年来陆续研发和上市了一系列抗HIV病毒的重磅药物,成为艾滋病医药市场的绝对霸主,近年来又因为其革命性的抗丙肝新药索非布韦一跃成为制药界巨星。知元团队认为,吉利德取得如此令人瞩目的成绩与其在相关领域进行了有效的产品组合及严密的专利布局,确保其市场独占性是密不可分的。
知元团队对吉利德在抗HIV病毒药领域的专利布局,特别是其在中国的专利布局进行了分析和研究,发现吉利德在中国的专利布局并非坚不可摧,如果仿制药企业能够及早对其专利信息充分分析,有可能在抗HIV病毒领域抢占先机。
从2001年TDF单方获批至今,吉利德共有12个抗HIV病毒药物获得FDA批准,包括2016年4月4日刚刚获批的DESCOVY。在这12个FDA批准的药物中,共有8个涉及复方[i]。而其中,恩曲他滨和TDF是这些复方的重要基酒。在2015年之前,吉利德获批的四个复方(分别是TRUVADA、ATRIPLA、COMPLERA和STRIBILD)中都含有恩曲他滨和TDF。2015年和2016年获批的四个复方中,有三个复方(分别是GENVOYA、ODEFSEY和DESCOVY)都是将已获批复方中的TDF直接替换成了TA或者TAF。从吉利徳这8个复方的组成变化能明显地发现,吉利德在2015年之后的药品申报策略已经调整为将已获批复方中的TDF换成TA或者TAF,作为新药报批上市。
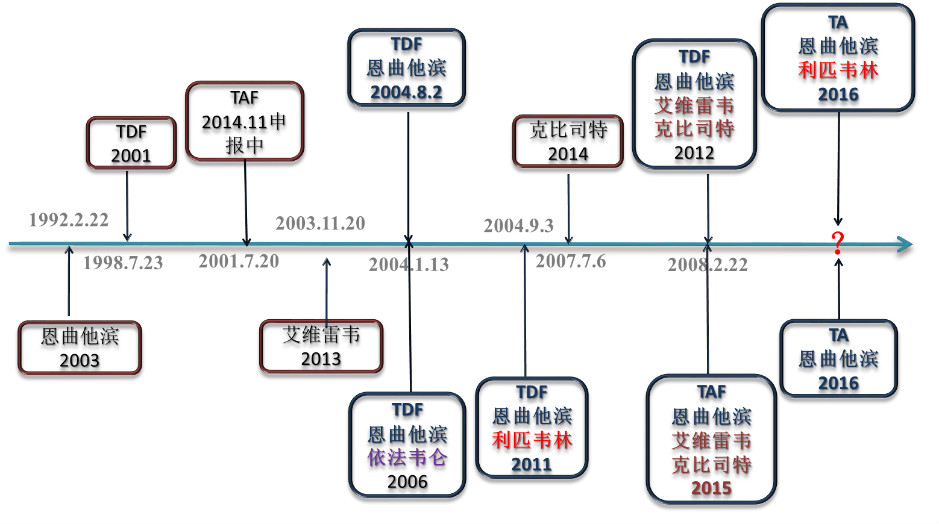 图例说明:每个框格中是上市药品的活性成分及其FDA批准时间,蓝色时间轴上标注的日期是上市产品对应的专利申请的提交时间。
图例说明:每个框格中是上市药品的活性成分及其FDA批准时间,蓝色时间轴上标注的日期是上市产品对应的专利申请的提交时间。
对于上述新药报批策略的调整,知元团队认为,这可能和两款药物的专利保护期有关。我们注意到,TDF即将于2018年7月23日期限届满,而TAF的原研专利将在2021年7月20日期限届满,而且该药物在美国和欧洲的专利保护期都分别被延长至2025年和2027年。
吉利德保护TA或者TAF的中国专利(ZL01813161.1)的申请日是2001年7月20日,公布日是2003年9月17日,其WO同族(WO02/08241A1)公布得更早(2002年1月31日)。该专利在说明书中明确记载,相对于TDF,TA的抗病毒活性增加了10倍并且在血浆中的稳定性增加了200倍。基于这两份专利公开的信息,且吉利德于2004年开始,获批了一系列的TDF复方药品。知元同创认为,如果仿制药企业能够及早关注到上述专利及吉利德新药获批的信息,应该非常容易想到用TA或者TAF尝试替换吉利德已获批复方中的TDF,从而可能抢先进行TA或者TAF联合用药的专利申请布局,甚至是药品申报。而不是在吉利德10年之后的2014年11月才开始陆续开展TA/TAF单方及复方的申报工作,并迅速从2015和2016年陆续获批3个复方。
在新化合物研发难度增大的现实下,国内药品生产企业应该对创新药物的开发风险有所准备,在药物研发模式中保留适当比例的“老药新用”、联合用药等已有药物的重开发。
企业在开发出新的联合用药后,如何进行专利保护呢?在不考虑“现有技术”状况的前提下,可采用以下三种主要类型的技术主题:
一、制药用途。例如:“含有TDF和恩曲他滨的组合物在制备治疗HIV感染的药物中的用途。”或者“TDF和恩曲他滨联合在制备治疗HIV感染的药物中的用途。”
二、药物组合物。例如:“一种药物组合物,其特征在于包含TDF和恩曲他滨。”
三、药物制剂。例如:“一种片剂,含有300mgTDF和200mg恩曲他滨、载体和赋形剂。”
具体到每个联合用药的技术方案,需结合现有技术状况、联合用药的改进点,选择适当的技术主题类型,必要时在相应权利要求中还要限定恰当的技术特征。
相对于申请文件的撰写,知元团队更希望指出的是:无论开发已有复方还是新复方,企业最好能结合专利分析开展自己的研发成果专利布局设计,从专利布局的方向、空间和时间角度出发,需要考虑例如以下的专利相关问题:
1、拟开发的复方是否有专利保护?
部分化合物的核心专利可以通过FDA橙皮书了解到,但从专利申请和侵权的角度,还需要进一步检索和查询是否存在其他类似或相关专利。
2、这些复方是否在目标区域有专利?
这是由于专利的地域性导致的,可能在美国有专利保护,但同样的药品在中国可能并没有专利,可以抢先进行仿制药的申报,此时在无专利保护的中国并不存在专利侵权风险。
3、这些复方的专利是否存在稳定性问题?
由于有些专利的稳定性存在问题,因为企业并非看到专利就绕开。最常规的做法是首先对于专利的稳定性进行分析。如果专利的稳定性确实存在问题,且成功无效的可能性较高,则企业可以进行复方研发,并在合适的时间提起专利无效。该做法在一定程度上,可以抢先进行仿制药的申报,并能够成功规避后续侵权风险。
4、原研公司是如何进行专利布局的?是否能够进行自己的专利布局?
前面提及的吉利德的HIV联合用药的布局就是非常好的示例,国内企业不仅可以学习和借鉴原研企业的专利布局经验,而且,如果通过分析能找到原研企业的专利布局缺陷,仿制药企业或能进行自己的专利布局。
知元团队尤其希望指出的是,国内企业在开发联合用药产品时,是否可以在更早期开始关注和研究专利文献?越早对竞争对手的专利信息开展分析,越有可能获得意外的先机。
[i] 8个复方的具体商品名及成分如下:
TRUVADA: TDF+恩曲他滨(F),TDF/F
ATRIPLA: TDF+恩曲他滨+依非韦伦,TDF/F/依非韦伦
COMPLERA: TDF+恩曲他滨+利匹韦林(R),TDF/F/R
STRIBILD: TDF+恩曲他滨+艾维雷韦+克比司特,TDF/F/E/C
PREZCOBIX: 地瑞拉韦+克比司特
GENVOYA: TAF+恩曲他滨+艾维雷韦(E)+克比司特(C),TAF/F/E/C
ODEFSEY: TA+恩曲他滨+利匹韦林,TA/F/R
DESCOVY:TA+恩曲他滨,TA/F
上一篇:【知元连载】化学药之化合物的专利布局与申请策略
下一篇:知元观点|瑞德西韦(Remdesivir)合成工艺的若干专利问题
